RESEARCH 研究概要
食塩による高血圧と臓器障害 Salt-induced hypertension and organ damage
食塩感受性高血圧及び食塩依存性腎障害の発症機序の解明
進化の過程において、脊椎動物が乾燥した陸上で生きていく上で腎臓におけるナトリウム再吸収機構は体液保持のために非常に重要でしたが、現代では過剰な食塩摂取が高血圧や腎臓病を発症させる原因となっています。高血圧は遺伝的素因の他、ストレスや肥満、加齢などの環境因子の影響を受けて発症しますが、食塩摂取が深く関与しています。食塩を摂取すると、血圧が上昇する人(食塩感受性)としない人(食塩非感受性)がいますが、食塩摂取により生じる高血圧を食塩感受性高血圧といいます。食塩感受性高血圧の人では、腎臓におけるナトリウム排泄機能に異常があるため、血圧を上昇させて圧利尿を促進することにより、腎臓からのナトリウム排泄を維持していると考えられています。
血圧調節には、交感神経系及び昇圧ホルモンカスケードであるレニン-アンジオテンシン-アルドステロン系(RAA系)が腎臓と連携して関わっており、本来RAA系は食塩摂取により抑制されますが、食塩感受性の個体においてはRAA系が交感神経系とともに不適切に亢進して血圧上昇や腎障害を発症します。例えばアルドステロンは腎臓でナトリウムの再吸収を促進するホルモンですが、通常、高食塩摂取時には分泌が抑制され、血圧は過度に上昇しないように調節されます。しかし、肥満などの病態ではアルドステロンが適切に抑制されず分泌し続けるため、食塩摂取時に血圧を上昇させるだけでなく、その受容体であるミネラロコルチコイド受容体(MR)の活性化を介して、心臓や腎臓の障害を生じることが分かりました。
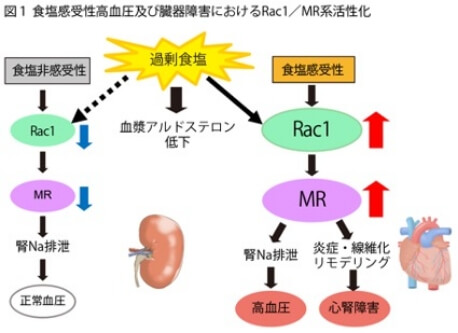
一方、食塩感受性高血圧を示す病態のなかには、食塩摂取時に血漿アルドステロン濃度が抑制されているにもかかわらず、MRが活性化され、高血圧や心腎障害を生じる現象が認められており、長年謎とされていました。その原因として、私達の研究により、食塩摂取時に腎臓でRac1蛋白が活性化され、MRを活性化するために高血圧や心腎障害を生じることが明らかになりました(Nat Med 2008, J Clin Invest 2011, Hypertension 2016 )。Rac1は低分子量Gタンパク質に属し、GDP結合型からGTP結合型への転換により活性型となり、特異的な標的分子に結合して細胞内シグナルを伝達する分子スイッチとして機能することが知られています。
また、さらなる研究により、Rac1は食塩摂取だけでなく、RAA系亢進下、糖尿病でも活性化し、MRの活性化を生じて高血圧や腎障害を生じることも明らかになりました(J Am Soc Nephrol 2012, Hypertension 2021)。食塩摂取が多い現代社会における高血圧や腎障害の治療法として、MR拮抗薬だけでなくRac1抑制薬は新たな治療標的になりうると考えられ、治療の有用性につき検討を重ねています(図1)。
加齢に伴う食塩感受性亢進と高血圧の発症機序
急速に高齢化が進み、我が国でも国民の4人に1人が高齢者です。また、加齢とともに高血圧の罹患率は上昇し、70代では7割以上が高血圧になります。加齢に伴い、血圧の食塩感受性が亢進することが知られていましたが、その機序はこれまで不明でした。一方、血中の抗加齢因子Klotho(クロトー)は加齢とともに減少することが知られていました。
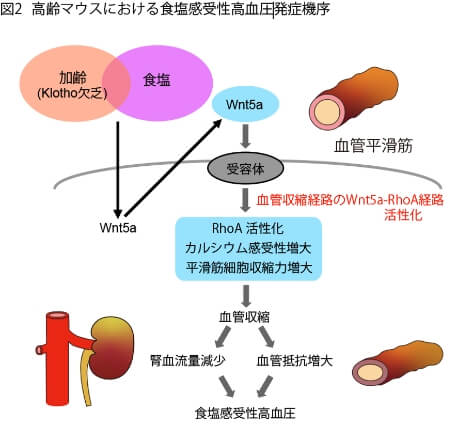
私達は、血中のKlothoが低下している高齢マウスを用いて、高食塩食を摂取すると、血管収縮経路であるWnt5a-RhoA経路が活性化して、血管収縮が亢進して高血圧を生じることを明らかにしました(J Clin Invest 2020)。この現象は食塩を摂取しないと生じず、血中Klothoが十分にある若いマウスでは生じません。すなわち、加齢に伴う高血圧は血中Klothoの低下という状況に高食塩摂取という生活因子が刺激となり生じることが明らかになりました。また、高齢者が若年者と異なり食塩感受性高血圧を呈する機序も明らかになりました。
さらに、一般に食塩感受性高血圧の患者では、高食塩摂取時に腎動脈の血管抵抗が増強して腎血流量が低下していることが知られていましたが、私達は高齢マウスの実験を通して、食塩摂取時の腎動脈のWnt5a-RhoA経路の収縮亢進が腎血流低下の機序として関与することを示しました。腎血流の低下は、結果的にレニン-アンジオテンシン-アルドステロン系や交感神経系の亢進により高血圧を生じます。これらのことから、加齢により、血中Klothoが低下した状況で高食塩を摂取すると、血管収縮経路であるWnt5a-RhoA経路の活性化が、全身の末梢血管や腎動脈で生じて血管収縮により血管抵抗が増大するとともに、腎血流も低下して、高血圧を発症すると考えられました。
さらに、高齢マウスの食塩感受性高血圧は、減塩や、血中Klothoの補充、Wnt阻害薬やRho活性化阻害薬により抑制されたことから、今後加齢性高血圧の新たな治療法となることも期待されます。
急速な高齢化社会を迎え、脳心血管病の最大リスクである高血圧の予防と治療は喫緊の問題です。私達の研究結果から、減塩が最大の予防法であることが示されました。また、Klothoは運動や肥満の回避などにより維持されることが知られており、生活スタイルの見直しも予防に重要であると考えられます。私たちは本研究を通して、加齢に伴う高血圧や腎機能障害の予防や新たな治療法の開発を行なう他、他の加齢性疾患への応用も検討しています。
Investigation of the pathogenesis of salt-sensitive hypertension and salt-dependent renal injury
During evolution, the sodium reabsorption mechanism in the kidneys was very important for vertebrates to survive on dry land for fluid retention, but today, excessive salt intake is a cause of hypertension and kidney disease. In addition to genetic predisposition, hypertension is influenced by environmental factors such as stress, obesity, and aging, but salt intake is deeply involved. Salt intake increases blood pressure (BP) in some people (salt-sensitive) and in others (non-salt-sensitive).We call hypertension that is caused by salt intake as salt-sensitive hypertension. In salt-sensitive hypertensive individuals, it is believed that sodium excretion from the kidneys is maintained by elevating BP and promoting pressure diuresis because of abnormal sodium excretion function in the kidneys.
The sympathetic nervous system and the renin-angiotensin-aldosterone system (RAAS), a hypertensive hormone cascade, are involved in BP regulation in cooperation with the kidneys, and the RAAS is originally suppressed by salt intake. However, in salt-sensitive individuals, the RAAS is also inappropriately elevated with the sympathetic nervous system during salt intake, resulting in elevated blood pressure and renal damage. Aldosterone, for example, is a hormone that promotes sodium reabsorption in the kidneys, but its secretion is normally suppressed during high salt intake and BP is regulated so that it does not rise excessively. However, in conditions such as obesity, aldosterone is not properly suppressed and continues to be secreted, resulting not only in increased BP during salt intake, but also in heart and kidney damage via activation of its receptor, the mineralocorticoid receptor (MR).
On the other hand, some conditions of salt-sensitive hypertension have been recognized as a phenomenon in which MR is activated during salt intake despite suppression of plasma aldosterone concentration, resulting in hypertension and cardiac and renal damage, which has been a mystery for many years. As a cause, our studies have revealed that Rac1 protein is activated in the kidneys during salt intake and activates MR, resulting in hypertension and cardiac and renal damage (Nat Med 2008, J Clin Invest 2011, Hypertension 2016). Rac1 belongs to a family of small G proteins and is known to become active by conversion from a GDP-bound to a GTP-bound form and to function as a molecular switch that binds to specific target molecules and transduces intracellular signals.
Further studies have also revealed that Rac1 is activated not only by salt intake, but also by hyperactivity of the RAA system and diabetes mellitus, resulting in MR activation, hypertension, and renal damage (J Am Soc Nephrol 2012, Hypertension 2021). Rac1 inhibitors as well as MR antagonists are potential new therapeutic targets for the treatment of hypertension and renal injury in today's salt-intensive society, and we are investigating their therapeutic potential (Fig. 1).
Mechanisms of Age-Related Increased Salt Sensitivity and Hypertension
With the rapid aging of the population, one out of every four people in Japan is an elderly person. The incidence of hypertension increases with age, and more than 70% of people in their 70s suffer from hypertension. It has been known that salt sensitivity of blood pressure increases with age, but the mechanism of this increase has been unknown. On the other hand, Klotho, an anti-aging factor in blood, was known to decrease with age. We have shown that high-salt diets activate the Wnt5a-RhoA pathway, a vasoconstrictor pathway, resulting in increased vasoconstriction and hypertension in aged mice with reduced Klotho in the blood (J Clin Invest 2020). This phenomenon does not occur without salt intake and does not occur in young mice with sufficient Klotho in the blood. In other words, it is now clear that age-related hypertension is caused by the decline of Klotho in the blood, which is stimulated by lifestyle factors such as high salt intake. The mechanism by which salt-sensitive hypertension develops in the elderly, as opposed to the young, was also clarified.
Furthermore, it is generally known that salt-sensitive hypertensive patients have decreased renal blood flow due to increased vascular resistance in renal arteries during high salt intake, but through experiments in aged mice, we have shown that increased contraction of the Wnt5a-RhoA pathway in renal arteries during salt intake is involved as a cause of decreased renal blood flow. Decreased renal blood flow results in hypertension due to the consequent enhancement of the renin-angiotensin-aldosterone system and sympathetic nervous system. These findings suggested that high salt intake in aged mice with decreased blood Klotho causes activation of the Wnt5a-RhoA pathway, a vasoconstrictor pathway, in systemic peripheral vessels and renal arteries, resulting in increased vascular resistance and decreased renal blood flow, leading to the development of hypertension.
Furthermore, salt-sensitive hypertension in aged mice was suppressed by salt reduction, blood Klotho supplementation, Wnt inhibitors, and Rho kinase inhibitors, which suggested these can be new therapies in age-related hypertension.
With the rapid aging of society, prevention and treatment of hypertension, the greatest risk for cerebrovascular disease, is an urgent issue. Our research results indicate that salt reduction is the greatest preventive measure. In addition, it is known that Klotho can be maintained through exercise and avoidance of obesity, and therefore, lifestyle modification is also considered important for prevention. Through this research, we are developing new methods for the prevention and treatment of age-related hypertension and renal dysfunction, and are also investigating the application of these methods to other age-related diseases.

