RESEARCH 研究概要
修復過程の理解に基づく治療 Therapy based on repair
ヒストンアセチル化酵素阻害による腎保護効果
腎疾患のなかでも慢性腎臓病は進行性である一方、急性の虚血性腎疾患では、腎臓は旺盛な再生能力を発揮します。腎臓還流が障害されて一過性に腎虚血になると腎臓の中でも酸素消費量の多い近位尿細管が壊死に陥り腎機能は著明に低下しますが、血流が早期に戻ると、一時的に透析療法が必要であったような症例でも腎機能はほぼ正常レベルまで回復します。この尿細管再生の過程では、胎児期に腎臓発生に関わったBMP7などの成長因子や転写因子が再誘導され腎臓の修復を促します。再誘導される因子は腎臓発生過程ではエピゲノムレベルの調節を受けているので、腎虚血後もエピゲノムが変化する可能性が考えられました。そこで私たちはヒストン修飾の中でも転写活性と関連のつよいヒストンH3K9Acがマウスの一過性腎虚血モデルで変化するか調べました。その結果、虚血になるとATP不足を反映してH3K9Acが虚血に弱い近位尿細管で一時的に減少し、血流再開後に徐々に元に戻ることが観察されました。このアセチルヒストンの回復にはHDAC5の減少が関与すること、さらにHDAC5の減少は成長因子BMP7の誘導に関わることが明らかになりました(J Am Soc Nephrol 19, 1311, 2008)。
内因性のHDAC5の減少が腎保護因子BMP7を増加させたため、私たちはHDAC阻害薬が腎保護効果を示すかどうか調べました。HDAC阻害薬トリコスタチンAは、培養尿細管細胞の実験(J Am Soc Nephrol 18, 58, 2007)、HDAC1, 2の増加がみられる尿管結紮モデル(Am J Physiol 298, F133, 2010)、糸球体腎炎モデル(Stem Cells 25, 2469, 2007)で抗線維化作用を発揮することが明らかになりました。HDAC阻害薬が上皮因子E-cadherinや、保護因子BMP7の遺伝子プロモーターのヒストンアセチル化促進させて、発現を保つことが一つの機序として考えられました。一方、炎症物質CSF-1の発現をHDAC阻害薬は抑制しており、ヒストンアセチル化を増加させる以外の作用も併せ持つと思われました。
内皮前駆様細胞による糸球体内皮の修復
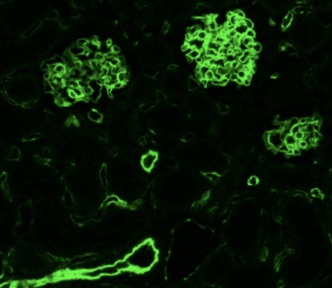
水電解質を制御する腎臓は血管に富んだ臓器で、血管内皮細胞を多く含みます(Fig. 4)。腎障害の際には内皮障害も生じています。そこで腎臓障害に対する内皮前駆細胞による内皮再生療法の効果を検討しました。骨髄から単核細胞を採取して内皮前駆様細胞に分化させ、糸球体腎炎ラットモデルに注入しました。細胞の注入により、糸球体の内皮障害、メサンギウム活性化、マクロファージ浸潤のいずれも改善しました。当初、注入した細胞が内皮細胞に分化して障害部位を補うと考えていましたが、実際のところ注入細胞が内皮になった像を呈するも箇所は少なく、注入細胞が内皮保護因子を産生することにより効果を示しているものと思われました(J Am Soc Nephrol 16, 997, 2005)。
Fig. 4
アルドステロンは血圧上昇作用とともに血管障害性に働くことが知られています。アルドステロンが内皮前駆細胞に及ぼす影響について調べたところ、アルドステロンは内皮前駆細胞への分化を濃度依存性に抑制することが明らかになりました。アルドステロンが内皮前駆細胞のVEGF受容体2を減少させることによりAktリン酸化が低下し、内皮前駆細胞の分化・増殖が不全になることが明らかになりました。抗アルドステロン薬による内皮保護作用の一つの機序に前駆細胞からの分化を保つことがあると考えられました(Hypertension 48, 490, 2006)。
Kidney protection by histone deacetylation inhibition
While chronic kidney disease is regarded as progressive in general, kidney function can recover almost completely after transient ischemia. During the period of recovery, proteins involved in nephrogenesis, including BMP7, are re-induced, and play important roles in kidney regeneration after ischemic injury. Given the critical role of epigenetic mechanisms in the induction and silencing of developmental genes during nephrogenesis, we reasoned that chromatin remodeling might somehow be modulated by ischemia. Since almost nothing had been reported with regard to epigenetic status in kidney disease at the time, we started by analyzing the levels of H3K9 acetylation, a histone mark which is tightly coupled with transcription. The levels of H3K9 acetylation decreased in response to ischemia especially in proximal tubular cells, the main target of ischemic injury due to high oxygen demand. In the recovery period, histone acetylation gradually increased. Recovery of histone acetylation was induced by decreased expression of histone deacetylase (HDAC) 5. Downregulation of HDAC5 led to an increased expression of BMP7 (J Am Soc Nephrol 19, 1311, 2008).
Since decrease of endogenous HDAC5 induced BMP7, a reno-protective molecule, we investigated whether HDAC inhibitors can exert reno-protective effects. Trichostatin A, an HDAC inhibitor, exerted anti-fibrotic effects in cultured renal tubular cells (J Am Soc Nephrol 18, 58, 2007), in the unilateral ureter ligation (Am J Physiol 298, F133, 2010) and glomerulonephritis models (Stem Cells 25, 2469, 2007). Preservation of E-cadherin and induction of BMP subsequent to histone acetylation of the promoter region may be involved in the protective effects. In addition, since HDAC inhibition reduced CSF-1, a chemoattractant, mechanisms other than histone acetylation of the promoter may also play a role.
Regeneration of glomerular endothelial cells by progenitor cells
Since the kidney regulates balance of water and electrolytes, it is enriched with vascular endothelial cells (Fig. 4). In kidney diseases, endothelial cells are damaged to some extent. Since bone marrow-derived cells were shown to protect endothelial injury, we investigated whether mononuclear cells obtained from the bone marrow exert protective effects against kidney injury. After their cultivation under a certain set of conditions to differentiate into endothelial progenitor cells, bone marrow-derived cells were injected into a model of glomerulonephritis in rats. Endothelial damage, mesangial activation, and inflammation of glomerulus were reduced by the injection. Endothelial growth factors produced by the injected cells were considered to play a major role in the protection (J Am Soc Nephrol 16, 997, 2005).
Aldosterone excess has been shown to induce vascular injury in addition to elevating blood pressure. We investigated the effect of aldosterone on differentiation of bone marrow mononuclear cells into cells with an endothelial progenitor phenotype. Aldosterone reduced VEGF receptor 2 expression, inhibited phosphorylation, and decreased formation of cells with endothelial phenotype. Aldosterone receptor antagonists may offer protection from vascular injury through differentiation of cells with endothelial progenitor phenotype (Hypertension 48, 490, 2006).

